- 3880 Aufrufe
„Die Aufgabe von Forschung ist es, gesellschaftlich relevante und drängende Fragen zu beantworten“, erklärt Roland Sauerbrey, Wissenschaftlicher Vorstand des Helmholtz-Zentrums Dresden-Rossendorf (HZDR). „Gerade unsere Krebsforschung leistet hier einen wichtigen Beitrag.“
Die Forscher am Dresdner Helmholtz-Zentrum befassen sich aber auch mit der effizienten und sicheren Nutzung von Energie und Ressourcen sowie mit der Untersuchung von Materie und Materialien unter extremen Bedingungen: Hohe Magnetfelder, Drücke und Temperaturen oder intensive Strahlung können verborgene oder unbekannte Eigenschaften von Materialien enthüllen. Das neue Wissen hilft bei der Optimierung von Werkstoffen oder eröffnet Wege für innovative Technologien. Dafür stehen den Dresdner Forschern, aber auch Kollegen aus aller Welt, einzigartige Anlagen wie das Ionenstrahlzentrum, das Hochfeld-Magnetlabor Dresden oder das ELBE-Zentrum für Hochleistungs-Strahlenquellen zu Verfügung. Neben seinem Hauptsitz in Dresden hat das HelmholtzZentrum Dresden-Rossendorf Standorte im französischen Grenoble sowie in Freiberg und Leipzig.
Ziel der Krebsforschung am HZDR ist es, Tumore besser sichtbar zu machen und zu charakterisieren sowie wirksamer zu behandeln. Eine der größten Herausforderungen an die Medizin im 21. Jahrhundert sind neue und effektive Krebstherapien. Das Messer des Chirurgen oder die ionisierende Strahlung im Rahmen einer Strahlentherapie finden im Kampf gegen den Krebs immer dann eine Grenze, wenn Tumore bereits gestreut und sich Absiedlungen (Metastasen) gebildet haben. Dann muss die Behandlungsmethode systemisch sein, das heißt, die Therapeutika müssen über die Blutbahn zu den Metastasen gelangen. Dies ist das Gebiet der Chemotherapie, wie sie heute bereits eingesetzt wird. Wesentliche Fortschritte bei der Therapie bestimmter Tumore könnten neue Arzneimittel, die Krebszellen entweder gezielt mit Radioaktivität oder über das körpereigene Immunsystem bekämpfen, bringen. Das HZDR verfolgt hier mehrere Wege. Erstes erforscht es spezielle, mit Radionukliden markierte Substanzen sowie Nanopartikel. Die Idee: Die Radionuklide werden mit einem Trägermolekül oder Trägerteilchen zum Tumor transportiert und die dort freiwerdende Strahlungsenergie führt zum Absterben der Krebszellen. Hierfür sind geeignete Radionuklide notwendig, die, am Wirkungsort angelangt, dort verbleiben müssen, bis die Strahlung abgeklungen ist. Dazu muss man geeignete Transportmoleküle oder -partikel finden, die in der Lage sind, an möglichst alle im Körper verstreuten Tumorzellen mit hoher Präzision anzudocken. Bei diesem Vorgehen darf die Strahlung nur möglichst wenig gesundes Gewebe schädigen.
Zweitens entwickeln Dresdner Forscher Arzneimittel, die Krebszellen mit Hilfe des körpereigenen Immunsystems vernichten sollen. Erste Krebsmedikamente dieses Typs, wie zum Beispiel „Blinatumomab“, sind bereits auf dem Markt, doch sie wirken jeweils nur gegen eine spezielle Krebserkrankung. Damit die gewünschte Immunreaktion im Körper noch besser funktioniert, werden am HZDR Antikörper konstruiert, die zwei Ziele erkennen können – also bispezifisch sind. Bindet so ein künstlicher, bispezifischer Antikörper sowohl an Krebs- als auch an Immunzellen, wird eine gezielte Immunreaktion gegen den Tumor ausgelöst. In der Bildgebung liegt der Fokus auf der Positronen-<wbr />EmissionsTomographie (PET). Für eine PET-Aufnahme wird dem Patienten eine radioaktiv markierte Substanz injiziert, die nach einiger Zeit zerfällt und dabei charakteristische Strahlung aussendet. Diese Photonen können von außen mit Hilfe einer Kamera gemessen und dank leistungsstarker Software in dreidimensionale Bilder umgerechnet werden.
Die laufende Entwicklung von Auswerte-Software zur Optimierung der Bildgebung ist ein wichtiges Anliegen der Rossendorfer Forscher. Im PET-Zentrum DresdenRossendorf werden an jedem Arbeitstag radioaktive Arzneimittel nach modernsten arzneimittelrechtlichen Methoden (GMP – Good Manufacturing Practice) hergestellt, die für die Anwendung am Patienten erlaubt sind und die sich in Tumoren und Metastasen anreichern. Hauptabnehmer ist das Universitätsklinikum Dresden. Zudem entwickeln die Wissenschaftler neue radioaktive Sonden, die dabei helfen sollen, Tumore genau zu charakterisieren. Eine neue Geräteklasse, welche die PET mit der Magnet-Resonanz-Tomographie (MRT) kombiniert, haben die Helmholtz-Forscher in enger Kooperation mit Ärzten des Dresdner Uniklinikums in die klinische Praxis überführt. Es handelte sich um Deutschlands erstes, für Patienten zugelassenes PET/MRT-Ganzkörpergerät, das im Jahr 2011 im HZDR den Betrieb aufnahm und an dem hier insgesamt mehr als 2.700 Patienten untersucht werden konnten. Seit kurzem befindet sich die Anlage auf dem Klinikgelände in unmittelbarer Nähe zum OncoRay-Zentrum, das gemeinsam vom HZDR, dem Universitätsklinikum Carl Gustav Carus Dresden und der gleichnamigen Medizinischen Fakultät an der Technischen Universität Dresden getragenen wird. OncoRay bildet zusammen mit dem HIRO-Institut am Deutschen Krebsforschungszentrum DKFZ und an der Universität Heidelberg das Nationale Zentrum für Strahlenforschung in der Onkologie und ist zudem Partner im Deutschen Konsortium für Translationale Krebsforschung.
Auch als neuer Standort des Nationalen Centrums für Tumorerkrankungen (NCT) zeigt Dresden, dass es mittlerweile neben Heidelberg einen zentralen Platz in der deutschen Krebsmedizin einnimmt. Mit dem NCT wird die Dresdner Universitätsmedizin ihre Forschungsanstrengungen zudem auf weitere Gebiete ausdehnen. Im OncoRay-Zentrum selbst steht der Einsatz von hochenergetischen Protonen in der Krebstherapie im Mittelpunkt. Dies geschieht hier patientennah und jenseits kommerzieller Zwänge. Jährlich erkranken fast 500.000 Patienten in Deutschland neu an Krebs. Aber jeder Patient, jeder Tumor ist anders. Nur mit individuellen Therapieansätzen kann die Heilungsrate, die derzeit bei etwa 50 Prozent liegt, weiter erhöht werden. Gerade die moderne Strahlentherapie hat schon einen relativ hohen Grad an Individualisierung erreicht, was auch auf die Fortschritte bei den Bildgebungsverfahren zurückzuführen ist. Damit lassen sich Tumore immer besser nachweisen, lokalisieren, deren Größe bestimmen und charakterisieren. Ein Beispiel ist das Auffinden von Tumorarealen, die besonders schlecht mit Sauerstoff versorgt sind. Diese sind resistenter gegen ionisierende Strahlung als gut durchblutete Tumorareale, weshalb Radioonkologen die Dosis hier gezielt erhöhen müssen.
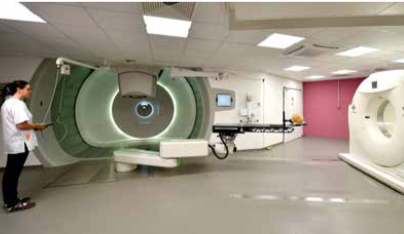
Von der Teilchentherapie mit Protonen, die seit Ende 2014 an der Universitäts Protonen Therapie Dresden (UPTD) angeboten wird, versprechen sich die Onkologen eine hochpräzise und zugleich besonders schonende Behandlung. 400 bis 500 Krebskranke im Jahr sollen hier behandelt werden (Disy berichtete in der letzten Ausgabe). Protonen sind positiv geladene Wasserstoff-Atome, denen zuvor ein Elektron entzogen wurde. Diese Teilchen werden auf hohe Energien beschleunigt und verhalten sich physikalisch völlig anders als Röntgenstrahlung, die üblicherweise in der Strahlentherapie genutzt wird. Für die Protonentherapie ist noch viel Forschungsarbeit zu leisten. Zum einen sind alle Patienten, die damit in Dresden behandelt werden, in wissenschaftlich kontrollierte, medizinische Studien integriert. Die Onkologen wollen so herausfinden, welche Patienten von der Teilchentherapie besonders profitieren. So werden zunächst vor allem Tumore im Hirn, an der Schädelbasis, des hinteren Bauchraums, des Beckens sowie Tumore bei Kindern und Tumore in vorbestrahltem Gewebe behandelt. Schätzungen zufolge könnten rund 15 Prozent der Krebspatienten von der Protonentherapie profitieren. Zum zweiten sind intensive Forschungsanstrengungen nötig, um die Bestrahlung in Echtzeit überwachen zu können. Dies ist bei Teilchenstrahlen besonders wichtig, weil sie auf einem nicht einmal stecknadelgroßen Punkt im Körper einen Großteil ihrer Energie abgeben. Für die Strahlentherapie mit ultraharter Röntgenstrahlung existieren aufgrund der jahrelangen Erfahrungen ausgefeilte Technologien, um eine optimale Bestrahlung zu gewährleisten. Diese lassen sich jedoch nicht auf die Protonentherapie übertragen. In einem gemeinsamen Forschungsprojekt arbeiten Wissenschaftler von HZDR und OncoRay an einer neuartigen Kamera, die in der Lage ist, den unsichtbaren Teilchenstrahl im Körper des Patienten sichtbar zu machen. Dabei nutzen sie aus, dass ein Teil der Protonen mit Atomkernen des bestrahlten Gewebes zusammenstößt. So kommt es zu Kernreaktionen, wodurch sekundäre Strahlungsarten, wie beispielsweise Gammastrahlung, Protonen und Neutronen, entstehen. Ziel ist es, den Radioonkologen Bilder an die Hand zu geben, auf denen genau abgebildet ist, wie viel Strahlendosis wo genau angekommen ist.
In Dresden sollen aber auch Hightech-Geräte entwickelt werden, die in Zukunft direkt bei der Behandlung eingreifen und korrigieren, wenn es zu Abweichungen zwischen der zuvor errechneten Strahlendosis oder der Reichweite des Protonenstrahles kommt. Für eine weite Verbreitung der neuartigen Therapieform sind noch viele Hürden zu nehmen. So wird für die Herstellung der Protonen ein großer Beschleuniger benötigt, der mit dicken Wänden von der Umgebung abgeschirmt werden muss. Dies gilt auch für das Strahlrohr zwischen Beschleuniger und Behandlungsplatz sowie den Behandlungsplatz selbst. Eine Anlage für die Protonentherapie ist deshalb sehr groß und teuer. Das wollen Physiker des Dresdner Helmholtz-Zentrums ändern. Sie arbeiten an einem kompakten Beschleuniger, der Protonen mit Hilfe eines Hochleistungslasers erzeugt. Im Gegensatz zum bisher benötigten Strahlenschutz wären die Maßnahmen für die Abschirmung deutlich geringer, aber auch die Anlage selbst könnte um rund die Hälfte schrumpfen – wodurch sich sicherlich auch die Kosten reduzieren ließen. Auch in Zukunft, da ist sich HZDR-Vorstand und Laserphysiker Roland Sauerbrey sicher, werden Wissen und Technologie „made in Dresden“ zur Heilung von Krebserkrankungen beitragen.















